4月23日 ,美国FDA加速批准Immunomedics公司的抗体偶联药物Trodelvy(sacituzumab govitecan-hziy),用于先前已接受过至少两种疗法治疗转移性疾病的转移性三阴性乳腺癌(mTNBC)成人患者。
值得一提的是,Trodelvy是FDA批准的第一个专门治疗复发或难治性mTNBC的ADC药物,也是FDA批准的第一个抗Trop-2 ADC药物。
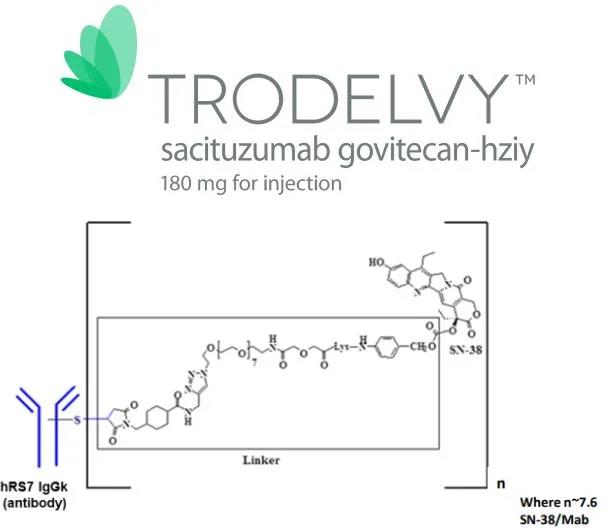
Trodelvy的活性药物成分为sacituzumab govitecan,这是一种新型、首创的抗体药物偶联物(ADC)药物,由靶向TROP-2抗原的人源化IgG1抗体与化疗药物伊立替康(一种拓扑异构酶I抑制剂)的代谢活性产物SN-38偶联而成。
简单来说,这款ADC药物,同时兼具了“生物导弹”的靶向作用和化疗的杀伤作用。
那什么是TROP-2抗原呢?
大家可能对TROP-2抗原不太熟悉,它是一种在90%以上的转移性三阴性乳腺癌中表达的细胞表面糖蛋白,与恶性肿瘤发生、侵袭和转移有关的癌基因。
由于其细胞外结构域在多种肿瘤上过表达,因此是靶向治疗发展的天然候选。另外,TROP-2的组织表达局限性使得治疗的毒性降低,这也是这款药物的优势所在。
该适应症的获批,是基于ASCENT的III期验证性研究(入组500例mTNBC患者)中取得的积极结果。
数据显示,Trodelvy治疗的客观缓解率(ORR)为33.3%(95%CI:24.6,43.1)、中位缓解持续时间(DOR)为7.7个月(95%CI:4.9,10.8)。
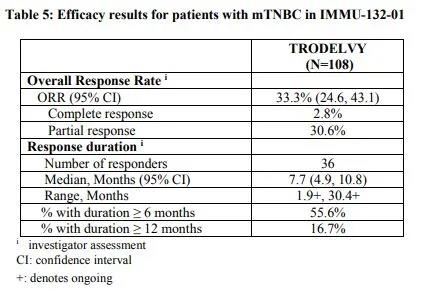
该研究在无进展生存期(PFS)、总生存期(OS)和客观缓解率(DOR)等取得优异的疗效。
乳腺癌是女性中最常见的癌症类型,全球每年确诊超过200万例。三阴乳腺癌(TNBC)约占所有乳腺癌比例的15%,与其他类型乳腺癌相比,TNBC在50岁以下女性中更为常见,进展迅速,预后极差,5年生存率不到15%。TNBC对激素疗法和抗HER-2靶向疗法无效,临床治疗选择非常有限,主要依靠化疗。
在这种治疗有限的情况下,Trodelvy有潜力成为TNBC治疗的一个标准护理药物,为三阴性乳腺癌患者带来了新药的希望!
本次FDA批准首个三阴性乳腺癌的ADC药物上市,将开辟三阴性乳腺癌晚期患者的新天地,期待它在我国的尽快上市!
常常去帮助,总是在安慰,康复之路易加医与您同行。如果您觉得这篇文章对您有帮助,欢迎关注易加医官网。易加医是专注于肿瘤领域的互联网医患平台,为肿瘤患者和家属提供涵盖肿瘤预防、就医、诊疗、康复所需的各类服务。



 浙公网安备 33010602004553号
浙公网安备 33010602004553号


