8月21日,中国国家药监局(NMPA)官网公示,通过优先审评审批程序附条件批准1类创新药氟泽雷塞片上市,该药适用于至少接受过一种系统性治疗的鼠类肉瘤病毒癌基因(KRAS)G12C突变型的晚期非小细胞肺癌(NSCLC)成人患者。

截图来源:NMPA官网
这是信达生物/劲方医药合作开发的KRAS G12C抑制剂。值得一提是,氟泽雷塞片是中国NMPA批准上市的首个KRAS抑制剂药物。
肺癌是全球发病率和死亡率最高的恶性肿瘤之一,其中非小细胞肺癌(NSCLC)是最常见的病理类型,约占所有肺癌的85%。KRAS突变是NSCLC中常见的驱动基因突变,约在25%的NSCLC患者中出现,约13%的患者携带KRAS G12C突变,该人群经过一线标准治疗进展后,可选择的二线治疗方案有限且有效率低,预后差。
氟泽雷塞是一款高效口服新分子实体化合物,通过共价不可逆修饰KRAS G12C蛋白突变体半胱氨酸残基,可有效抑制该蛋白介导的鸟苷三磷酸(GTP)/鸟苷二磷酸(GDP)交换,从而下调KRAS蛋白活化水平。此外,该产品抑制KRAS蛋白后,可进而抑制下游信号传导通路,有效诱导肿瘤细胞凋亡及细胞周期阻滞,达到抗肿瘤效果。

本次氟泽雷塞的获批是基于一项在中国开展的临床 II 期单臂注册研究结果。该研究旨在评估 IBI351 单药在标准治疗失败或不耐受且携带 KRAS G12C 突变的晚期 NSCLC 患者中的安全性、耐受性和疗效。
氟泽雷塞的 II 期注册临床研究(NCT05005234)数据显示:
- 氟泽雷塞显示出优异的抗肿瘤活性。独立影像学评审委员会(IRRC)评估的确认的客观缓解率(ORR)达 49.1%,达到了预设的主要终点;疾病控制率(DCR)达 90.5% 。值得一提的是,氟泽雷塞的 ORR 高于此前已获批的两款 KRAS G12C 抑制剂——安进的索托拉西布(ORR 为 32.7%)、百时美施贵宝的阿达格拉西(ORR 为 43%)。
- 中位缓解持续时间(DoR)为 8.3 个月,中位无进展生存期(mPFS)为 9.7 个月,中位生存期(OS)尚未达到。在 mPFS 方面,索托拉西布为 5.4 个月,阿达格拉西为 6.9 个月,也低于氟泽雷塞。
- IBI351 总体耐受性良好。
研究认为,氟泽雷塞展现出了令人鼓舞的疗效和可控的安全性。这些结果支持氟泽雷塞单药治疗可作为晚期 KRAS G12C 突变 NSCLC 患者的新治疗选择。
众所周知,KRAS是癌症中最常见的基因突变之一,也在过去几十年被公认为是“难以成药”靶点。直至近十年,针对KRAS蛋白的药物研发开始迎来转机,并在近几年诞生了首批获批的KRAS靶向疗法,例如Lumakras(sotorasib)和Krazati(adagrasib),为肿瘤患者带来了新的治疗手段。此次氟泽雷塞片在中国获批上市,也为中国特定肺癌患者带来了新的治疗选择。
小编也盘点了KRAS靶点突变相关的临床招募,成功入组有机会免费用药!有需要可以添加文末小助手咨询。
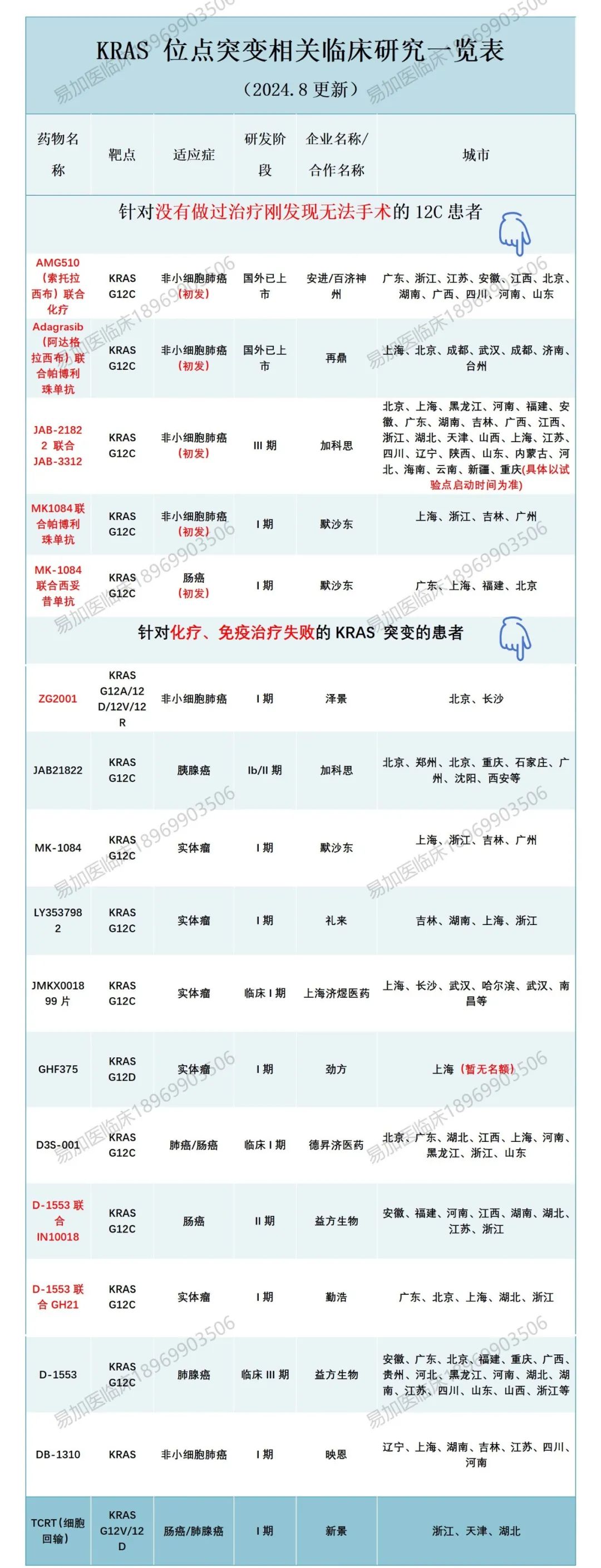
肿瘤患友若想了解氟泽雷塞的价格及慈善赠药信息或者KRAS相关临床招募,欢迎添加下方二维码咨询。也可加入“阳光易家亲–KRAS突变肿瘤患友群”,与上万位肿瘤患友/家属分享经验,互通有无。




 浙公网安备 33010602004553号
浙公网安备 33010602004553号


